Door Marcel Muskiet (ma.muskiet@vumc.nl)
Cardiovasculair voordeel van een nieuw glucose-verlagend medicijn in een cardiovasculaire veiligheidsstudie (CVOT) in type 2 diabetes. Voor de EASD in 2015 (Stockholm, Zweden) een uitkomst die nog haast voor onmogelijk werd gehouden, gegeven: 1) de non-inferiority doelstelling (en designs) van CVOT’s, en 2) enigszins teleurstellende neutrale resultaten van 4 -op dat moment- gepubliceerde trials. Het was daarom dat de sterk positieve cardiovasculaire uitkomsten van EMPA-REG OUTCOME (SGLT2 remmer empagliflozine) met verbazing en opwinding werden ontvangen in 2015. Sinds vorige week buigt de diabetesgemeenschap zich over de inmiddels 4e positieve CVOT; de 2e waarin een SGLT2 remmer werd onderzocht: CANVAS (canagliflozine). De CANVAS-resultaten werden gepresenteerd op de 77ste Scientific Sessions van de ADA in San Diego, en kwamen direct daarna online in New England Journal of Medicine.
Hoe verhouden de voor- en nadelen van canagliflozine en empagliflozine zich in hun respectievelijke CVOT’s? Kunnen we spreken van een klasse-effect van de SGLT2 remmers? Wat is de klinische betekenis van de uitkomsten van CANVAS en EMPA-REG OUTCOME? De discussie zal ongetwijfeld op grote schaal losbarsten – hieronder een aanzet tot een beschouwing.
Klasse-effect?
In grote lijnen lijkt het ‘CANVAS programma’ (gecombineerde data uit hoofdstudie CANVAS en de renale-eindpunt studie CANVAS-R) de eerder getoonde cardiovasculaire en renale voordelen van empagliflozine in EMPA-REG OUTCOME te bevestigen. “Het is waarschijnlijk dat we kunnen spreken over een gunstig klasse-effect van de SGLT2 remmers op cardiovasculair en renaal risico in type 2 diabetes”, aldus onafhankelijk commentator Prof. Clifford J. Bailey (Aston University, Birmingham, UK), na afloop van de data-presentatie.
Canagliflozine ≠ empagliflozine?
De mate waarin canagliflozine en empagliflozine als glucose-verlagende medicijnen uitwisselbaar zijn is allerminst duidelijk. Er zijn opmerkelijke verschillen in studieresultaten tussen de twee CVOT’s, die primair kunnen samenhangen met verschillen in b.v. studie-design/-populatie, en daarmee een directe vergelijking van de middelen formeel onjuist maakt. De verleiding om te vergelijken is echter groot, daar de consequenties voor de klinische praktijk potentieel groot zijn. Zo is er de suggestie van klinisch relevante PK/PD verschillen tussen de twee SGLT2 remmers (o.a. de uiteenlopende selectiviteit voor SGLT2 ten opzichte van SGLT1; canagliflozine 160:1 vs empagliflozine 5000:1).
Cardiovasculair: 3-point MACE vs. individuele componenten
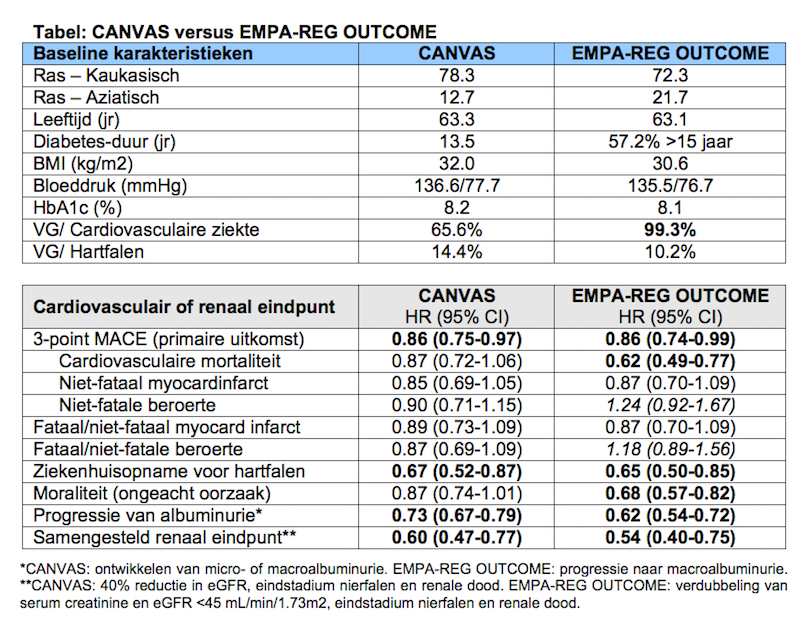
Canagliflozine reduceerde het risico op het primaire, samengestelde cardiovasculaire eindpunt (3-point MACE; cardiovasculaire mortaliteit, niet-fataal myocardinfarct en niet-fatale beroerte) met 14% na gemiddeld 188 weken (3.6 jaar). Opvallend genoeg, na 3.1 jaar in EMPA-REG OUTCOME, was het risico op MACE in de empagliflozine-groep eveneens met 14% gedaald ten opzichte van placebo. Echter, geen van de individuele componenten van de 3-point MACE was statistisch significant gereduceerd met canagliflozine, waar empagliflozine nog een opvallend voordeel van maar liefst 38% (95% CI 23-51%; P<0.001) op cardiovasculaire mortaliteit toonde. Dit voordeel in EMPA-REG OUTCOME was voor de US FDA, na een spannende stemming in juni 2016 (11 tegen 12 stemmen), reden om het productlabel van empagliflozine te voorzien van de tekst “geïndiceerd voor cardiovasculaire mortaliteit in patiënten met type 2 diabetes en cardiovasculaire ziekte”. De superioriteit van canagliflozine op MACE is met P=0.02, in een enkele studie, waarschijnlijk onvoldoende substantieel bewijs om een soortgelijke claim door de US FDA goedgekeurd te krijgen. De potentieel meest nadelige uitkomst in EMPA-REG OUTCOME was een niet significante stijging van 24% in niet-fatale beroerte (HR 1.24; 95% CI 0.92-1.67). Daarentegen, veel events in de empagliflozine-arm deden zich voor > 90 dagen na inname van de laatste studiemedicatie (18 versus 3 events). In een post-hoc analyse (recent gepubliceerd in Stroke), bleek er geen relatie tussen het optreden van een beroerte en 1) mate van hematocriet-stijging, en 2) sterke daling in systolische bloeddruk met empagliflozine. CANVAS stelt op dit punt eveneens gerust; het risico op niet-fatale beroerte met canagliflozine lag met de puntschatting aan de goede kant van het risico-spectrum (HR 0.90; 95% CI 0.71-1.15). Prof. Bailey wees erop dat in EMPA-REG OUTCOME alle geïncludeerde patiënten reeds een cardiovasculair event hadden doorgemaakt, terwijl dit slechts 65.6% van de patiënten in CANVAS betrof. “EMPA-REG OUTCOME bestudeerde patiënten met mogelijk verder gevorderde ziekte, terwijl CANVAS relatief dichter bij de populatie ligt zoals deze in de huisartsenpraktijk wordt gezien”, aldus Bailey. Dus, mogelijk is het cardioprotectieve effect in CANVAS verwaterd door het beduidend lager baseline cardiovasculair risico in deze studie. Desalniettemin suggereert de data wel ook in een combinatie van hoog- en (relatief) laag-risico patiënten het cardiovasculaire voordeel van een SGLT2 remmer groter is dan standaard behandeling.
Renoprotectie – primair versus secundair
Beide studies toonden indrukwekkend renaal voordeel van SGLT2 remming, daarbij in acht genomen dat reeds 80% van de patiënten reeds een RAAS remmer kregen voorgeschreven. Empagliflozine verlaagde het risico op het samengestelde renale eindpunt met 39% (95% CI 30-47%), bestaande uit macroalbuminurie, verdubbeling van serum creatinine, eindstadium nierfalen (ESRD), en renale dood. Indien macroalbuminurie (een surrogaat eindpunt) uit dit eindpunt werd gehaald, bleef een sterk significant voordeel op harde renale eindpunten bestaan. Echter, renale eindpunten waren secundair/exploratief in EMPA-REG OUTCOME, en de methodologie bij het vaststellen van de renale events kreeg nadien enige kritiek te verduren.
CANVAS-R daarentegen, als onderdeel van het CANVAS programma, had albuminurie als primair eindpunt. Canagliflozine verlaagde het risico op albuminurie-progressie met 27%, en het samengestelde renale eindpunt met 40% (95% CI 23-53%), bestaande uit “40% reductie in eGFR”, ESRD en renale dood. Echter, “40% reductie in eGFR” is nog altijd een betwist eindpunt in klinische studies, en heeft slechts geringe klinische waarde. Om de betekenis van de individuele eindpunten, alsmede het beloop van eGFR over de tijd, in te schatten zal gewacht moeten worden op de renale paper die zal volgen uit CANVAS/CANVAS-R. Daarnaast, de resultaten van de volledig toegewijde renale uitkomst studie met canagliflozine (CREDENCE; NCT02065791) in 4,200 type 2 diabetes patiënten met diabetische nierziekte worden verwacht in 2019.
Amputaties en fracturen – onoverkomelijke problemen?
Ondanks de cardiovasculaire en renale voordelen van canagliflozine in CANVAS, werd het enthousiasme gedrukte door het 97% (95% CI 41-175%) verhoogde risico op amputaties van tenen, (voor)voeten en (in mindere mate) onderbenen (6.3 versus 3.4 events per 1000 patiënt-jaren). Het hoogste risico werd gevonden in patiënten met een eerdere amputatie, of perifeer vaatlijden, maar het risico was ongeacht voorgeschiedenis verhoogd. Canagliflozine veroorzaakte bij 15 meer patiënten per 1000 het ontstaan van een amputatie over een periode van 5 jaar. Om deze uitkomst in perspectief te zetten: canagliflozine verlaagde de incidentie van MACE per 1000 patiënten over 5 jaar met 23, hospitalisatie voor hartfalen met 16 per 1000, en renale events met 17 per 1000. Daarnaast, doch minder op de voorgrond, verhoogde canagliflozine het risico op fracturen met 26% (15.4 versus 11.9 per 1000 patiënt-jaren; P=0.02) in CANVAS, maar niet in CANVAS-R.
In EMPA-REG OUTCOME was er geen sprake van een toegenomen aantal amputaties of fracturen, maar deze data werd niet zo specifiek of zorgvuldig verzameld als in CANVAS. Desalniettemin is het risico op amputaties van dusdanige zorg dat de EMA in februari 2017 een “black-box” waarschuwing liet optekenen op de bijsluiters van alle beschikbare SGLT-2 remmers in Europa. De potentiele onderliggende mechanismen, al dan niet specifiek voor canagliflozine, zijn (vooralsnog) onbekend. Aan de ander kant zijn er ook deskundigen die twijfelen aan de medicijnafhankelijkheid van de negatieve bevinding. Wordt ongetwijfeld vervolgd…
Canagliflozine versus empagliflozine voor de praktijk
De resultaten van CANVAS en EMPA-REG OUTCOME pleiten tezamen een voordelig klasse-effect van SGLT2 remmers op cardiovasculair en renaal risico. Een directe vergelijking tussen canagliflozine en empagliflozine is zoals gezegd formeel niet mogelijk, gegeven de verschillen tussen de twee CVOT’s qua design en populatie. Desniettemin, de ernst van de potentiele complicaties (amputaties en fracturen) met canagliflozine in CANVAS wegen zwaar ten opzichte van het potentiele voordeel op MACE in het algemeen. Voordat er meer duidelijkheid is over de eventuele vermijdbaarheid van deze bijwerkingen in CANVAS zullen artsen zeer waarschijnlijk terughoudend zijn om de voorkeur te geven aan canagliflozine boven empagliflozine.
Contact
Marcel H.A. Muskiet, arts-onderzoeker
VU Medisch Centrum Amsterdam
Diabetescentrum, Afdeling Interne Geneeskunde
Telefoon: 020-4442780
Email: ma.muskiet@vumc.nl
Conflicts of interest
MM is consultant voor Eli Lilly & Co. en NovoNordisk (alle honoraria worden uitgekeerd aan werkgever VUmc).