Diabetische perifere neuropathie (DPN) is een veelvoorkomende complicatie van zowel diabetes type 1 als 2. Het is de belangrijkste oorzaak van de ontwikkeling van diabetische voetulcera, van niet-traumatische amputaties van de onderste ledematen en het kan leiden tot verminderde balans en ernstige neuropathische pijn, die vaak niet reageert op therapie. De diagnose DNP wordt in de meeste gevallen pas in een al gevorderd stadium gesteld. Hoe kan eerder worden gediagnosticeerd om veel leed te voorkomen?
Een belangrijk gegeven is dat 80% van DPN-gerelateerde amputaties te voorkomen zijn door middel van goede multidisciplinaire zorg die niet alleen het risico op amputaties vermindert, maar ook het risico op ziekenhuisopname en het ontstaan van nieuwe voetulcera aanzienlijk verlaagt.1
Diagnose
Voor de diagnose van DNP worden in de regel het 10 g monofilament gebruikt, de Ipswich Touch test , de trillingstest met de Vibratip, een stemvork of geautomatiseerde apparaten als de vibratie sensorische analysator VSA-3000, de Neurometer , en de biothesiometer. Hiermee wordt met name de sensatie getest en het risico op voetulcera. Deze tests diagnosticeren DNP meestal in een gevorderd stadium van de aandoening. Intensievere multifactoriële interventie in een vroeg stadium zou de gevolgen van DPN kunnen voorkomen.
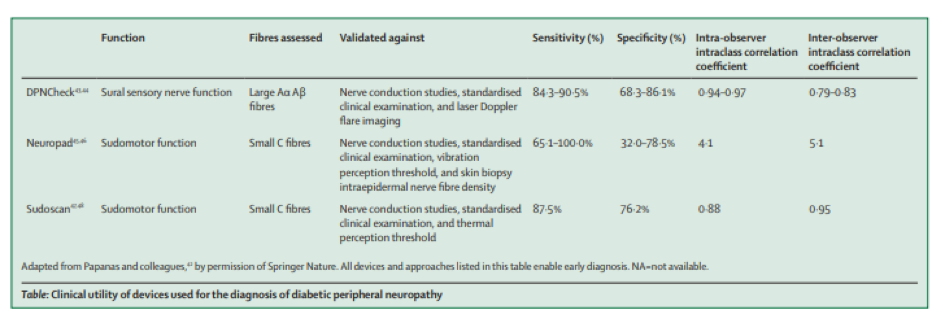
Er zijn onderzoeken gedaan om inzicht te krijgen in de eventuele meerwaarde van innovatieve Point-of-Care-hulpmiddelen, zoals de DPNCheck, de Neuropad en de Sudoscan.
- DPNCheck is een instrument waarmee in 3 minuten de zenuwgeleiding kan worden vastgesteld met zeer grote betrouwbaarheid. De DPNCheck heeft 95% gevoeligheid en 71% specificiteit in vergelijking met een referentiestandaard zenuwgeleidingonderzoek voor de diagnose van DPN.12,
- De Neuropad is een 10-minuten test die de zweetproductie op de zool van de voet meet. Het is gebaseerd op een kleurverandering van blauw naar roze. De gevoeligheid van de Neuropad is hoger dan die van het 10 g monofilament (95%) en de biothesiometer (73%).
- De Sudoscan meet wat de betrokkenheid is van de kleine vezels bij DPN.,, De meting is gebaseerd op een elektrochemische reactie tussen elektroden en chloride-ionen na stimulatie van zweetklieren door laagspanningsstroom.
Geconcludeerd kan worden dat de gevoeligheid van POCD’s aanvaardbaar is voor detectie; een combinatie van hulpmiddelen voor analyse van zowel de dunne als de dikke vezels moet worden gebruikt om DPN te kunnen vaststellen Studies met POCD’s zijn relatief klein en er is een hoge heterogeniteit. De meerwaarde in de klinische praktijk is nog niet duidelijk. Verdere studies zijn nodig om de prestaties van elke afzonderlijke POCD te beoordelen.
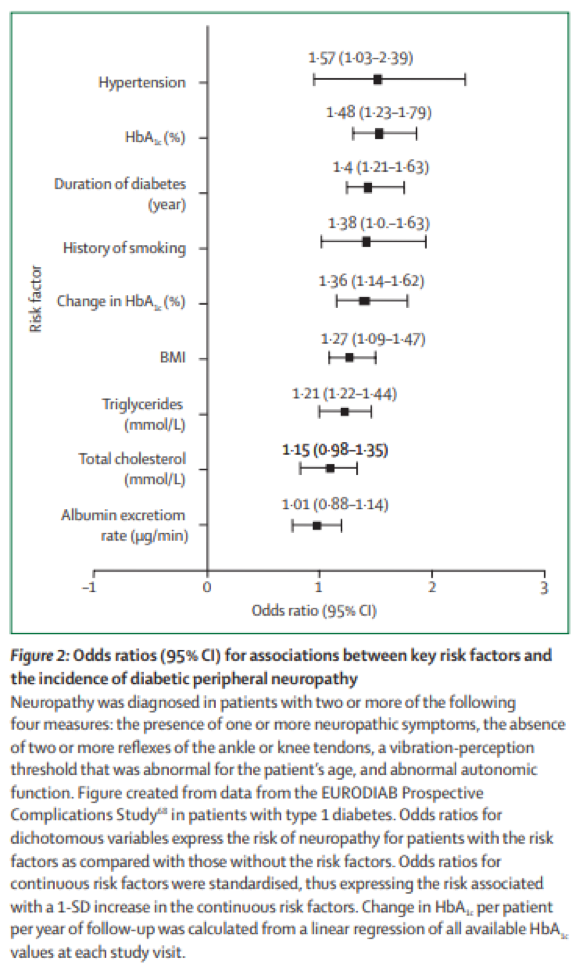
De belangrijkste factor voor het ontstaan van DPN zijn hyperglykemieën, maar er zijn meer factoren van invloed. De EURODIAB-studie heeft aangetoond dat er bij mensen met diabetes type 1 ook cardiovasculaire risicofactoren zijn als triglyceriden, overgewicht, hypertensie en roken (figuur 2). Recent zijn in de ADDITION-studie ook bij mensen met diabetes type 2 soortgelijke cardiovasculaire risicofactoren aangetoond.
One-stop-service
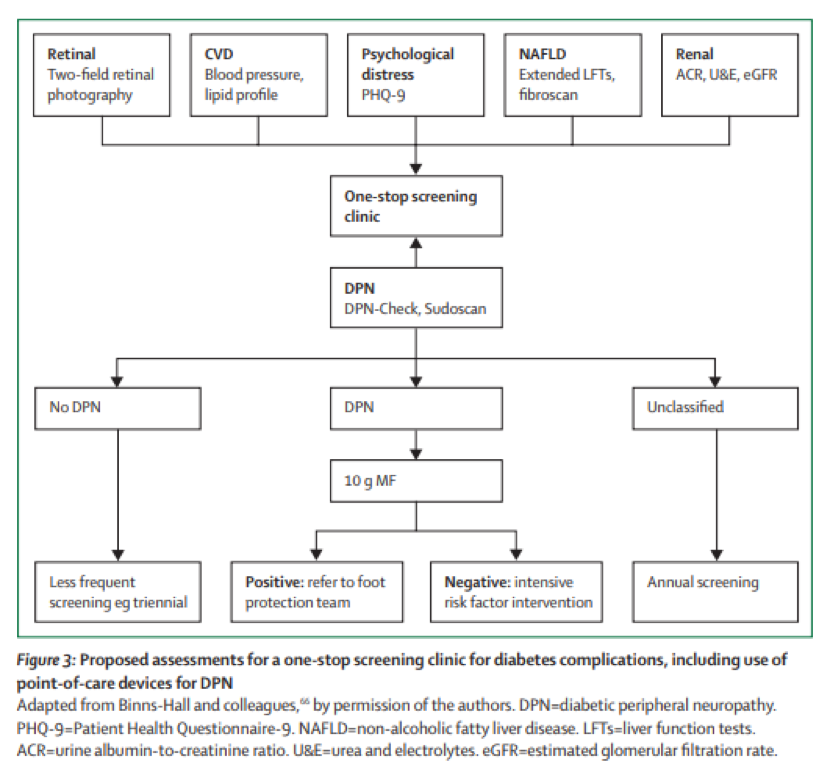
Recent is een zgn. one-stop-service voor het screenen van complicaties getest in de eerste en tweede lijn in het Verenigd Koninkrijk. Een getrainde podoloog deed gedetailleerde beoordelingen van het risico op voetulcera en gebruikte hierbij instrumenten voor het screenen van de kleine en grote zenuwvezels (DPNCheck en Sudoscan) voor de diagnose van subklinische DPN. Deze pilotstudie onderzocht ook de haalbaarheid en aanvaardbaarheid van een one-stop-service voor gecombineerde screening voor alle diabetesgerelateerde microvasculaire complicaties. Deze gecombineerde screening van oog-, nier-, DPN-en voetulcera verminderde het aantal ziekenhuisbezoeken, leidde tot een vroegtijdige diagnose van DPN (93.2% gevoeligheid voor de diagnose van DPN) en pijnlijke DPN. Dit model is effectief voor de vroege diagnose van DPN en het management van voetcomplicaties.
Verder onderzoek moet aantonen of intensief management van cardio-metabole risicofactoren voor patiënten met beginnende subklinische DPN, vastgesteld met behulp van POCD’s, de ontwikkeling van klinische DPN kan voorkomen of verergering van de ziekte kan stoppen.
Bron: Dinesh Selvarajah D, et al. PhD Diabetic peripheral neuropathy: advances in diagnosis and strategies for screening and early intervention. Lancet Diabetes & Endocrinology, October 14, 2019
Referenties
- Singh, N, Armstrong DG, Lipsky BA. Preventing foot ulcers in patients with diabetes. JAMA 2005; 293: 217–28.
- Boulton AJM, Armstrong DG, Kirsner RS, et al. Diagnosis and Management of Diabetic Foot Complications. Arlington (VA): American Diabetes Association; 2018.
- Feng Y, Schlösser FJ, Sumpio BE. The Semmes Weinstein monofilament examination as a screening tool for diabetic peripheral neuropathy. J Vasc Surg 2009; 50: 675–82. 29 Rayman G, Vas PR, Baker N,
- Rayman G, Vas PR, Baker N, et al. The Ipswich Touch Test: a simple and novel method to identify inpatients with diabetes at risk of foot ulceration. Diabetes Care 2011; 34: 1517–18.
- Bowling FL, Abbott CA, Harris WE, Atanasov S, Malik RA, Boulton AJ. A pocket-sized disposable device for testing the integrity of sensation in the outpatient setting. Diabet Med 2012; 29: 1550–52.
- Richard JL, Reilhes L, Buvry S, Goletto M, Faillie JL. Screening patients at risk for diabetic foot ulceration: a comparison between measurement of vibration perception threshold and 10-g monofilament test. Int Wound J 2014; 11: 147–51.
- Santos TRM, Melo JV, Leite NC, Salles GF, Cardoso CRL. Usefulness of the vibration perception thresholds measurement as a diagnostic method for diabetic peripheral neuropathy: Results from the Rio de Janeiro type 2 diabetes cohort study. J Diabetes Complications 2018; 32: 770–76.
- Inceu GV, Veresiu IA. Measurement of current perception thresholds using the Neurometer—applicability in diabetic neuropathy. Clujul Med 2015; 88: 449–52.
- Park JH, Won JC. Patterns of nerve conduction abnormalities in patients with type 2 diabetes mellitus according to the clinical phenotype determined by the current perception threshold. Diabetes Metab J 2018; 42: 519–28.
- Azzopardi K, Gatt A, Chockalingam N, Formosa C. Hidden dangers revealed by misdiagnosed diabetic neuropathy: a comparison of simple clinical tests for the screening of vibration perception threshold at primary care level. Prim Care Diabetes 2018; 12: 111–15.
- Weisman A, Bril V, Ngo M, et al. Identification and prediction of diabetic sensorimotor polyneuropathy using individual and simple combinations of nerve conduction study parameters. PLoS One 2013; 8: e58783
- Lee JA, Halpern EM, Lovblom LE, Yeung E, Bril V, Perkins BA. Reliability and validity of a point-of-care sural nerve conduction device for identification of diabetic neuropathy. PLoS One 2014; 9: e86515
- hatzikosma G, Pafili K, Demetriou M, Vadikolias K, Maltezos E, Papanas N. Evaluation of sural nerve automated nerve conduction study in the diagnosis of peripheral neuropathy in patients with type 2 diabetes mellitus. Arch Med Sci 2016; 12: 390.
- Didangelos T, Zografou I, Iliadis F, Sambanis C. Validation of Neuropad in the assessment of peripheral diabetic neuropathy in patients with Diabetes Mellitus versus the Michigan Neuropathy Screening Instrument, 10 g Monofilament application and Biothesiometer measurement. Curr Vasc Pharmacol 2019; published online July 23. DOI:10.2174/1570161117666190723155324
- Selvarajah D, Cash T, Davies J, et al. SUDOSCAN: a simple, rapid, and objective method with potential for screening for diabetic peripheral neuropathy. PLoS One 2015; 10: e0138224.
- Mao F, Liu S, Qiao X, et al. Sudoscan is an effective screening method for asymptomatic diabetic neuropathy in Chinese type 2 diabetes mellitus patients. J Diabetes Investig 2017; 8: 363–68.
- Mayaudon H, Miloche PO, Bauduceau B. A new simple method for assessing sudomotor function: relevance in type 2 diabetes. Diabetes Metab 2010; 36: 450–54.
- Grisold A, Callaghan BC, Feldman EL. Mediators of diabetic neuropathy: is hyperglycemia the only culprit? Curr Opin Endocrinol Diabetes Obes 2017; 24: 103–11
- Binns-Hall O, Selvarajah D, Sanger D, Walker J, Scott A, Tesfaye S. One-stop microvascular screening service: an effective model for the early detection of diabetic peripheral neuropathy and the high-risk foot. Diabet Med 2018; 35: 887–94