De prestigieuze ‘Banting Lecture’ op de ADA werd dit jaar gehouden door Professor Ele Ferrannini uit Pisa. Vooral bekend om zijn werk op het gebied van insulineresistentie, wist hij toch een brug te slaan naar insulinesecretie door bèta-cellen, de ontdekking die een eeuw geleden door Banting en Best leidde tot de behandeling van diabetes met insuline.
In de jaren 80 publiceerde Ferrannini in de NEJM een studie bij personen met hypertensie, die een normale glucosetolerantie hadden en een negatieve familieanamnese voor diabetes. Daarbij vond hij dat hypertensie gepaard gaat met insulineresistentie. Later heeft hij met zijn team in Pisa, in samenwerking met vele teams in USA en Europa, insulineresistentie onderzocht in verschillende weefsels bij mensen met diabetes en ook bij andere groepen patiënten zonder diabetes.
Het meest bekend is insulineresistentie op het niveau van de spieren: 70% van ons glucoseverbruik is door spieren. Dit blijkt geen gevolg te zijn van verminderde doorbloeding of van shunting, maar van een verminderde fractionele extractie van glucose door het spierweefsel: 20% in plaats van 35%.
Ook in vetweefsel is er insulineresistentie; dit hangt samen met de insulineresistentie in de spieren: bij minder glucoseoxidatie wordt er meer vet geoxideerd. Dit is het gevolg van meer lipolyse en daarbij komen meer vrije vetzuren in de bloedbaan. Alle soorten en localisaties vetweefsel tonen hetzelfde patroon: veel minder glucose uptake en meer lipolyse.
Vetoxidatie is ook toegenomen in de lever, hier gaat dit samen met toegenomen glucoseproductie. De toegenomen glucoseproductie wordt veroorzaakt door toegenomen gluconeogenese, niet door glycogenolyse. De toegenomen lipolyse leidt tot meer vrije vetzuren (en soms ketonlichamen) , die deels geoxideerd kunnen worden, maar na re-esterificatie deels in de lever opgeslagen worden (steatose/NASH) en deels weer in de circulatie terecht komen als triglyceride-rijke lipoproteïnen (VLDL).
Ook het hart blijkt insulineresistent bij T2DM: m.b.v. FPG-PET scan techniek werd een verminderde glucose uptake gezien ondanks een goede doorbloeding. Dit was gecorreleerd met een verminderde ejectiefractie.
Als laatste orgaan werd de vaatwand bestudeerd: personen met DM 2 hebben een verminderde vasodilatatie door acetylcholine bij insulineresistente T2DM in vergelijking met normale glucosetolerantie; dat betekent dat er vanuit het endotheel minder vasodilaterende NO geproduceerd wordt.
Ongeveer 15 jaar geleden verschoof de aandacht naar insulinesecretie
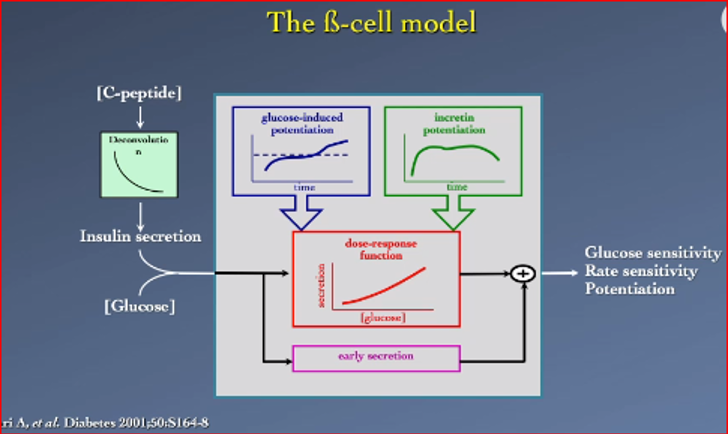
Bij zowel T1DM als bij T2DM konden Ferrannini en zijn groep aan de hand van oGTT’s en insulinespiegels tijdens een oGTT een model maken van bèta-cel insuline gevoeligheid: de insuline secretiesnelheid versus de bloedglucose; moderators in dit model zijn effecten van incretinen, de eerste fase secretie en glucose afhankelijke potentiering.
Mari et al, Diabetes 2001; 50: S164-8
Bij post-bariatrische chirurgie konden ze met dit model aantonen dat naast afname van insulineresistentie in perifere weefsels (na 40 kg vermagering) er ook een daadwerkelijke toename van insuline secernerende capaciteit was en dat er dus daadwerkeklijk gesproken kan worden van diabetes remissie in een aantal gevallen.
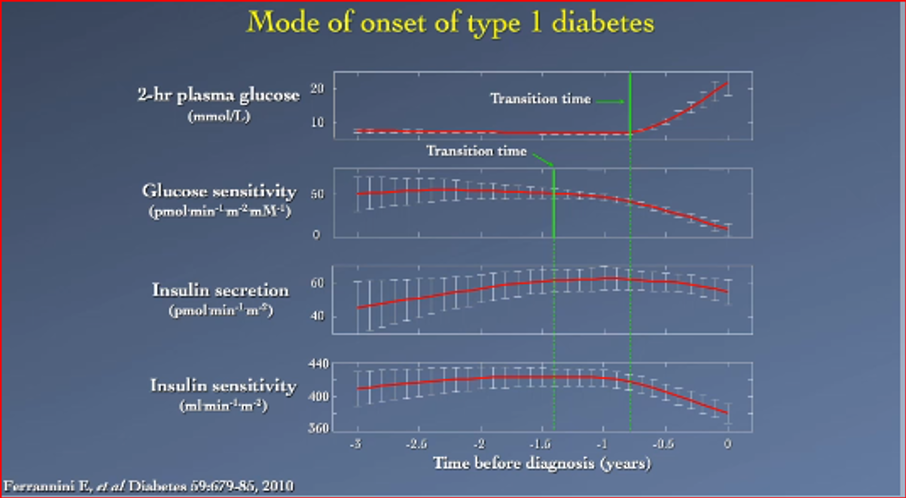
Ook bij T1DM werd dit model onderzocht: in samenwerking met de Amerikaanse groep van de DPT studie, waarin personen at risk voor T1DM (positieve GAD en positieve familieanamnese) jaarlijks met een oGTT werden gevolgd vond de groep van Ferrannini dat driekwart jaar voor de diagnose DM 1 de plasma glucose bij oGTT stijgt, maar dat anderhalf jaar voor de diagnose diabetes al de bèta-cel insuline gevoeligheid daalt.
Ferrannini, Diabetes 2010; 69: 679-86
Voor Ele Ferrannini eindigt de zoektocht niet en met een knipoog naar COVID-19 besluit hij zijn laatste dia: